Sistemul imunitar
Sistemul imunitar constituie întregul departament al apărării din corp. Acesta cuprinde o mare varietate de celule, anticorpi, proteine și substanțe chimice care acționează împreună împotriva inamicului.
Sistemul imunitar este împărțit în două sisteme complementare, dar diferite de apărare:
- Sistemul imunitar înnăscut, denumit și sistemul imunitar nespecific.
- Sistemul imunitar adaptiv, denumit și sistemul imunitar specific sau dobândit.
Imunitatea celulară este parte a sistemului imunitar adaptiv și este mediată de un tip de celule albe numite celule T sau limfocite T. Acestea se formează în măduva osoasă și sunt eliberate în sânge încă din faza de imaturitate. Celulele T călătoresc spre timus și se maturizează în interiorul glandei. Odată maturizate în timus, ele se deplasează către alte locuri din corp prin sânge și prin sistemul limfatic. Timusul eliberează în corp două clase importante de celule T, diferențiate prin două glicoproteine încorporate în membranele lor celulare. Aceste glicoproteine sunt numite CD4 și CD8 (CD= cluster de diferențiere) care acționează asemenea unor corectori pentru receptorul celulei T, însemnând că lucrează împreună cu receptorul celulei T pentru recunoașterea invadatorilor străini.
Există numeroase tipuri diferite de celule T ce pot fi clasificate în funcție de prezența CD4 sau CD8 (iar în unele cazuri, de absența acestora) în membrana lor celulară:
- Celulele T citotoxice (celule T Killer) sunt celule T CD8+ care atacă celulele corpului infectate de virusuri și anumite bacterii.
- Celulele T ajutătoare sunt un tip de celule CD4+ și sunt principalii reglementatori ai defensivei imunității adaptive. Ele nu pot omorî celulele infectate sau curăța patogenii, ci mai degrabă coordonează răspunsul imunității prin direcționarea altor celule care să le execute sarcinile. Celulele T ajutătoare sunt activate de sistemul imunitar înnăscut prin prezentarea antigenului și, odată activate, ele se vor diviza rapid și vor elibera citokine (mesageri chimici ai inflamației). Anumite subtipuri diferite de celule T ajutătoare pot fi formate, incluzând Th1, Th2, Th3, Th9, Th17, Th2, Tr1 și Tfh. Fiecare subtip secretă diferite categorii de răspunsuri imunitare.
Cele mai importante celule T ajutătoare pentru acționarea sistemului imunitar și a inflamației sunt celulele Th1, Th2, Th9, Th17 și Th22.
Celulele Th1 recrutează și reglementează celulele imune nespecifice, cum sunt macrofagele, și secretă citokine ce stimulează maturizarea celulelor T în celule T citotoxice.
Celulele Th2 activează celulele B, ce se vor diviza rapid și vor secreta anticorpi.
Celulele Th9 sunt similare cu celulele Th2, fiind activate de citokine diferite și sunt importante pentru apărarea împotriva infecțiilor parazitare, dar sunt implicate și în dezvoltarea inflamațiilor alergice cronice, în remodelarea căilor respiratorii (astmul bronșic) și în boala autoimună.
Celulele Th17 sunt extrem de inflamatorii și sunt activate ca răspuns la anumite bacterii și paraziți. Numărul excesiv de celule Th17 activate este responsabil pentru leziunile tisulare și anumite boli autoimune, incluzând artrita reumatoidă, scleroza multiplă și sindromul inflamator intestinal.
Celulele Th22 sunt asemenea celulelor Th1 și sunt implicate în tulburările inflamatorii ale pielii, cum sunt psoriazisul, dermatita atopică și dermatica alergică de contact.
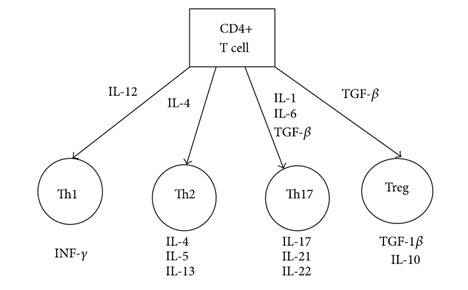
Diferențierea celulelor T CD4+ (Sursa: http://www.hindawi.com/journals/jir/2015/979167/ )
Echilibrul Th1/Th2
Se crede că prezența sau activarea celulelor Th1 și Th2 relativă are un efect de reglare asupra comportamentului imunitar. Până de curând, suprimarea relativă a celulelor Th1 prin creșterea relativă a activității celulelor Th2 era considerată a fi un mecanism principal de menținere sau restabilire a echilibrului într-un sistem imunitar bolnav. În zilele noastre, totuși, un subset specializat de celule T reglatoare este considerat responsabil pentru principalele efecte ale asigurării unui sistem imunitar echilibrat. Este posibil ca proteinele de șoc termic (hsp) să fie antigeni relevanți care conduc la o astfel de reglementare.
Proteinele de șoc termic sunt cunoscute a fi antigeni imunodominanți ai bacteriilor. Sunt proteine puternic conservate din punct de vedere evolutiv, prezente în toate organismele celulare eucariote și procariote și sunt suprareglate de mai multe forme de stres. În ciuda autotoleranței, epitopii hsp omologi cu secvențele hsp ale gazdei endogene au fost implicați ca epitopi de celule T pentru a dota celulele T reactive încrucișate, specifice hsp, cu capacitatea de a regla inflamația, cum ar fi în bolile autoimune induse experimental. S-a descoperit că astfel de celule T produc citokine reglatoare, cum ar fi IL10, în contrast cu celulele T induse cu alte proteine microbiene conservate care nu sunt suprareglate de stres. Hsp au fost implicate în reglarea imună nu numai ca ținte reglate în sensul superior al imunității adaptive în timpul stresului inflamator, dar recent și ca factori declanșatori ai imunității înnăscute prin activarea prin intermediul receptorilor Toll-like.
Ce înseamnă dominanța Th1 sau Th2?
Se crede că unul dintre factorii care contribuie la boala autoimună este dezechilibrul dintre subtipurile de celule T ajutătoare. Mai exact, anumite boli autoimune tind să fie asociate cu o supraactivare a celulelor Th1 sau Th2, cunoscută ca dominanța Th1, respectiv Th2. Totuși, nu este o regulă generală. De exemplu, tiroidita Hashimoto este deseori, dar nu întotdeauna, asociată cu dominanța Th1. La fel de bine există și tiroidită Hashimoto cu dominanță Th2. Chiar mai mult, dominanța se poate transforma foarte repede și ușor ca răspuns la o varietate de stimuli, cum ar fi starea nutrițională (anumite deficiențe sau surplusuri de diferiți micronutrienți pot cauza o schimbare a dominanței Th1 în Th2 și invers).
Cât de importantă este dominanța Th1 versus Th2 în ceea ce privește dezvoltarea sau tratamentul bolii rămâne un mister, mai ales că identificarea altor celule T ajutătoare indică faptul că sistemul imun este mult mai complicat decât s-a crezut la început. Anumiți profesioniști din domeniul medicinei alternative aplică strategii ce vizează stimularea celulelor Th1 sau Th2 (în funcție de care dintre ele prezintă un nivel mai scăzut, lucru determinat prin analize de sânge) pentru a reface „echilibrul“ sistemului imunitar (ceea ce, uneori, are și rezultate, deoarece celulele Th1 și Th2 se suprimă unele pe celelalte). Totuși, dezechilibrul celulelor Th1 și Th2 reprezintă, de asemenea, un indicator pentru inadecvarea sau ineficiența celulelor Th3, Tr1 și T de reglementare, care nu sunt luate în considerare în cazul acestor strategii de „echilibrare a imunității“. În plus, aceste strategii nu țin cont de contribuția celulelor Th9, Th17 și Th22.
Echilibrul dintre Th1 și Th2 (și chiar dintre Th9, Th17 și Th22) poate fi obținut și prin reducerea inflamației din corp, prin înlăturarea factorilor declanșatori ai sistemului imunitar și prin sprijinirea producției și activității celulelor Th3, Tr1 și a celulei T de reglementare sănătoase (Treg).
Rolul Th17 în patogeneza tiroiditei Hashimoto
Tiroidita Hashimoto a fost mult timp asociată epidemiologic cu excesul de iod. Cu toate acestea, mecanismele imunologice de bază rămân în mare parte neexplorate. Celulele Th17 sunt recunoscute în mod obișnuit că joacă roluri vitale în diferite boli autoimune. Studiile ar arătat că celulele Th17 care se infiltrează intratiroidian și nivelurile serice de IL-17 au fost semnificativ crescute la pacienții cu Hashimoto. Cu toate acestea, concentrația de IL-17 seric a fost invers corelată cu funcția tiroidiană reziduală a pacienților, în timp ce IL-17 tiroidian exprimat eterogen a fost corelat direct cu fibroza locală. S-a constatat că administrarea de niveluri moderate de iod facilitează polarizarea celulelor T naive splenice murine în celule Th17, în timp ce nivelurile extrem de ridicate de iod au favorizat polarizarea Th1 și au inhibat dezvoltarea Treg. Aceste descoperiri sugerează că atât celulele Th1, cât și Th17 pot fi implicate în patogeneza tiroiditel Hashimoto și nivelurile ridicate de iod pot juca un rol critic în acest proces prin modularea diferențierii celulelor T.
Concluzii
În ciuda diferitelor cercetări efectuate în ultimii ani, patogeneza tiroiditei Hashimoto nu este încă pe deplin înțeleasă. Nu există nicio îndoială că limfocitele Th1 participă la dezvoltarea acestei boli, dar se pare că ele nu joacă un rol atât de important pe cât se credea. Mai mult, semnificația participării subgrupurilor de CD4+ nou descoperite, cum ar fi Th17, în etiopatogenia tiroiditei Hashimoto este încă discutabilă. Multe teste în vitro demonstrează o funcție esențială a Treg în tulburările autoimunologice. Diverse studii efectuate pe modele animale arată o corelație puternică între scăderea numărului sau afectarea funcției celulelor T reglatoare și dezvoltarea tiroiditei. În plus, infuzia de limfocite de la șoareci maturi sănătoși a prevenit dezvoltarea acestor tulburări. De asemenea, se pare că realizarea eutiroidiei prin oprirea inflamației la nivelul tiroidei duce la încetarea autoagresiunii, ceea ce încurajează funcționarea corectă a celulelor T reglatoare.
SURSE:
http://pubmed.ncbi.nlm.nih.gov/10666776
http://pubmed.ncbi.nlm.nih.gov/24211715
http://www.elsevier.es/en-revista-endocrinologia-nutricion-12-articulo-pathogenesis-thyroid-autoimmune-disease-role-S1575092216300468
http://www.hindawi.com/journals/jir/2015/979167
Dr. Sarah Ballantyne – Metoda Paleo. Combate bolile autoimune și vindecă-ți organismul












